關於樂和
乐于心,和与众,与己乐,与人和; 心宽念纯,百病无生。


全球範圍內常見的惡性腫瘤之一,據2020年全球癌症統計,食管癌的新發病人數達60.4萬,死亡人數達54.4萬。中國是食管癌高發地區,隨著早診和治療技術的發展,中國食管癌的死亡率呈下降趨勢,早期食管癌5年生存率可達90%以上,但由於大多數患者診斷時已是中晚期,此時的治療效果仍然不佳,總體5年生存率僅在20%左右,依舊是威脅我國居民健康的主要惡性腫瘤。
大量飲酒、吸煙、亞硝酸鹽、食管反流、吃熱食、喝熱水等與食管癌有關。遺傳因素也很重要,家族中如果直系親屬或者多個親屬患有食管癌,那麼應該定期查體及避免高危因素的接觸。當然了,即便是普通群體,也應該盡量摒除上述習慣和對症治療。

Overview of the illness
1. 趙先生病理分期為ⅡB期,已存在淋巴結轉移,此種情況單純手術切除的復發概率極高,所以術後應積極進行輔助治療,進一步清除殘餘腫瘤細胞,達到控制腫瘤復發的目的。
2. 多個研究認為,術後輔助放療可改善接受單純手術後淋巴結陽性病人的預後,且放療聯合化療效果優於單純放療。當前食管癌術後輔助治療通常採用以化療為主的治療方式,但對食管癌患者而言,化療有效率很低,治療效果較差,客觀緩解率僅6%-8%,只能在短期內可對腫瘤細胞產生殺傷抑製作用,且存在耐藥現象;另外化療的副作用顯著,對免疫系統、造血系統具有嚴重的損傷作用,不能獲得長治久安的效果,所以不是理想的術後輔助治療方式。
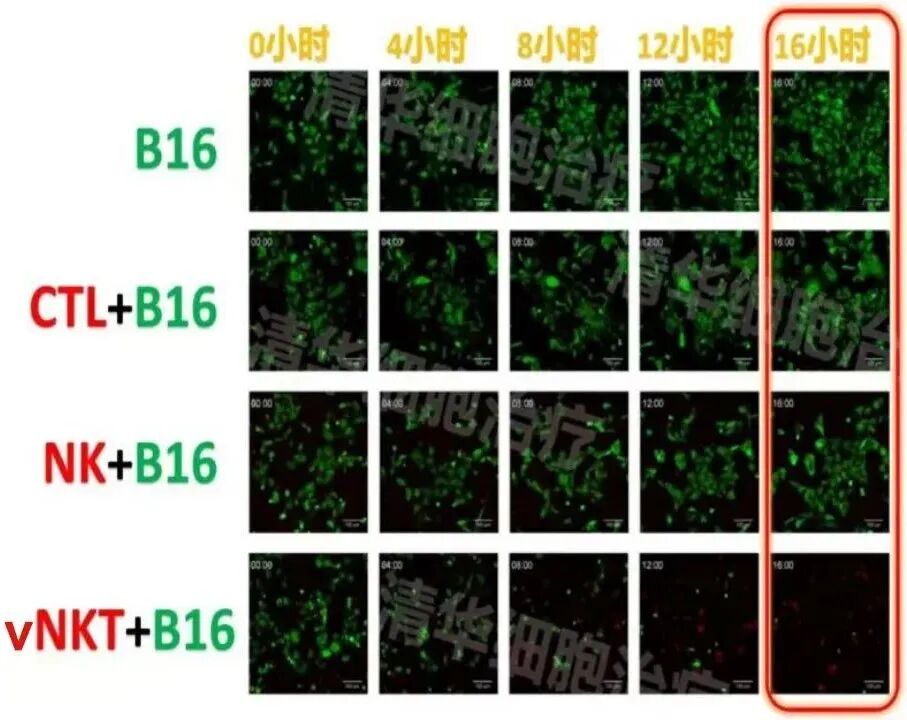
實驗條件:有vNKT細胞存在的情況下,經過16個小時,近乎所有B16腫瘤細胞被殺死!
張教授向趙先生及家人詳細介紹了vNKT治療技術及既往案例的治療成果,並對趙先生的疑問進行了詳細解答。經過充分溝通,趙先生及家人一致認可樂和團隊關於腫瘤治療的“戰略”思想和“戰術”規劃,於2022年3月7日開始vNKT細胞治療。第一階段治療方案:1療程/月,2023年7月調整為1療程/2月,目前已完成16療程(截止到2024年10月)。目前隨訪病情穩定,未見復發及轉移徵象,現患者精神狀態良好,食慾睡眠俱佳,生活質量良好。
影像學改變
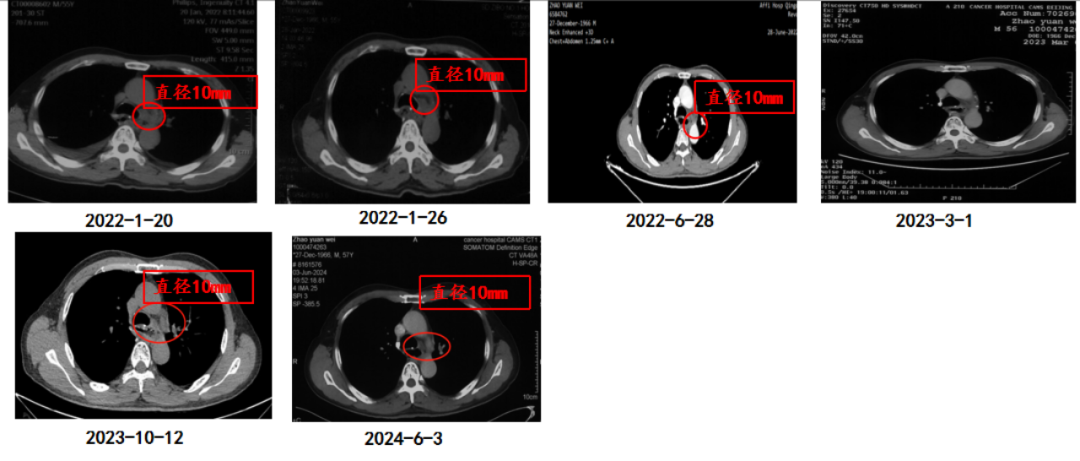
Conclusion and Commentary
術後復發,是所有經歷手術治療的惡性腫瘤患者都最為擔心的問題,也是腫瘤獲得治癒的最大障礙,所有腫瘤手術治療後都存在不同程度的復發幾率,尤其是發現時分期較晚,腫瘤較大,惡性程度較高的腫瘤。趙先生術後病理提示存在淋巴結轉移,術後復發幾率很高,按照傳統治療方案,術後應接受放化療,但趙先生在瞭解到放化療的局限性以及對身體的損傷作用後,否認了這一治療方式。
在經過科學分析比較後,最終選擇了進行vNKT細胞治療,治療至今已平穩度過3年,達到了理想的治療效果。在這個過程中vNKT細胞免疫治療在降低復發轉移的風險中扮演了一個不可或缺的角色,為患者獲得腫瘤長期穩定甚至治癒提供可能性。



掃描二維碼
與張明徽教授團隊溝通

點擊圖片查看往期精彩內容
