關於樂和
乐于心,和与众,与己乐,与人和; 心宽念纯,百病无生。

Overview of the illness
2018年9月的常規體檢改變了張女士的人生軌跡。胃鏡檢查發現賁門胃底黏膜異常,經病理確診為賁門胃底腺癌。

首次治療選擇創傷較小的內鏡黏膜下剝離術(ESD),這種微創手術雖能保留胃部結構,但相較於根治手術存在局限——就像清除表土下的雜草,難以徹底鏟除深部根系。
有研究表明:ESD與外科手術治療早期胃癌的總生存率無顯著差異,但無復發生存率顯著低於外科手術組[1]術後病理提示隱患:癌細胞已侵及粘膜下層,為兩年後的復發埋下伏筆。
2020年9月,消瘦、食慾減退等警報信號伴隨CA724指標飆升至20+(正常值<6.9 U/mL)再次拉響復發警報。胃鏡復查證實腫瘤復發,這次不得不接受根治性全胃切除術。
術後病理結果顯示為低分化腺癌,浸潤漿膜層,並可見脈管內癌栓及神經侵犯,淋巴結轉移癌(5/22)。基因檢測示:MET14號外顯子跳躍突變。
術後,張女士開始了3週期的SOX方案化療。然而,化療的副作用很快顯現——惡心、嘔吐、乏力接踵而至,最讓她痛苦的是,剛做完手術消化功能很弱,“每次吃飯都像打仗,吃一口吐兩口 ”。營養狀況差是張女士後續化療不耐受的重要原因。
2021年2月,復查顯示骨髓抑制嚴重,醫生不得不將方案調整為單藥替吉奧。儘管副作用有所減輕,但營養跟不上影響了化療的耐受性,最終在2021年6月,因骨髓抑制無法緩解,治療再次中斷,後改用PD-1抑制劑(信迪利單抗)治療至今。
化療藥物作為細胞毒性藥物,通過干擾細胞分裂和增殖來殺滅癌細胞。然而,化療藥物無差別攻擊的特性誤傷了那些分裂活躍的正常細胞,如骨髓中的造血細胞,從而引發骨髓抑制。

與此同時術後病理提示的高危因素協同放大,低分化腺癌,脈管內癌栓及神經侵犯及淋巴結轉移都提示預後較差。
在傳統治療手段接連受挫後,張女士一度陷入迷茫。化療做不了,靶向藥又用不上,難道只能等待再次復發嗎?
在通過張明徽教授的樂和新醫學團隊瞭解到vNKT細胞治療機制和優勢後,張女士認為該方法非常適合她當前的身體狀況和治療需求。
1. 雙重殺傷機制:vNKT細胞兼具NK細胞的快速殺傷能力和T細胞的精准識別能力,能夠高效鎖定並清除癌細胞,同時避免對正常細胞的傷害。
2. 天然安全性:作為人體天然存在的免疫細胞,vNKT細胞未經基因工程改造,因此副作用較小,患者耐受性良好,尤其適合化療不耐受的患者。
3. 協同增效作用:vNKT細胞能夠重塑腫瘤微環境,延緩PD-1抑制劑的耐藥出現,實現1+1>2的治療效果。
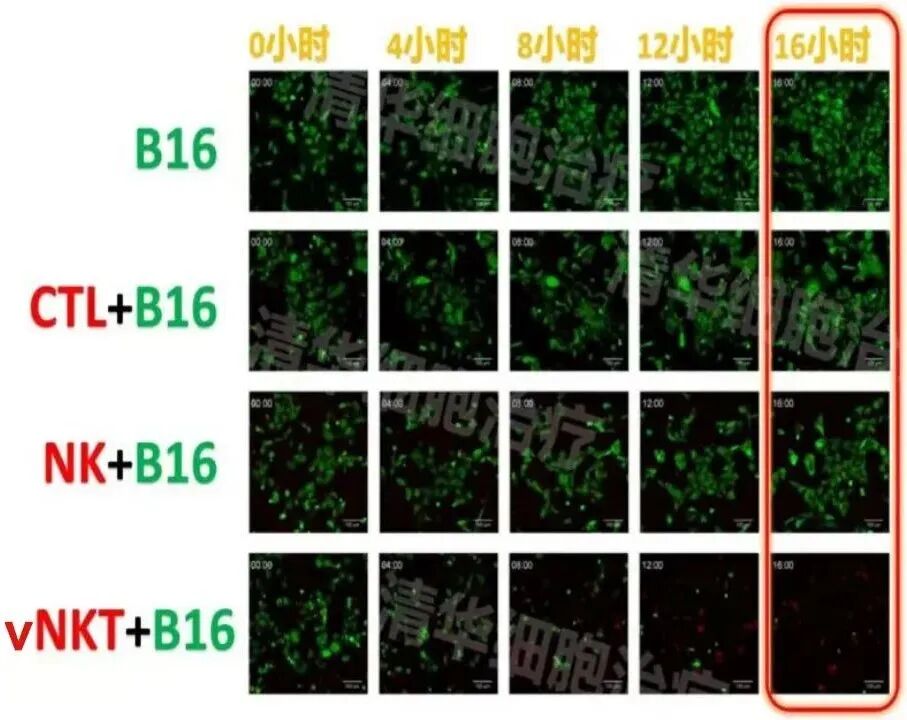
實驗條件:有vNKT細胞存在的情況下,經過16個小時,近乎所有B16腫瘤細胞被殺死!
自2022年4月25日起,張女士開始接受vNKT細胞治療,截至2024年3月12日已完成15個療程。經過系統治療,她的病情顯著改善,影像學隨訪未見異常,腫瘤標誌物穩定,已實現4年無復發生存。生活質量明顯提升,精神狀態良好,精力充沛,日常生活完全恢復正常。
影像學改變
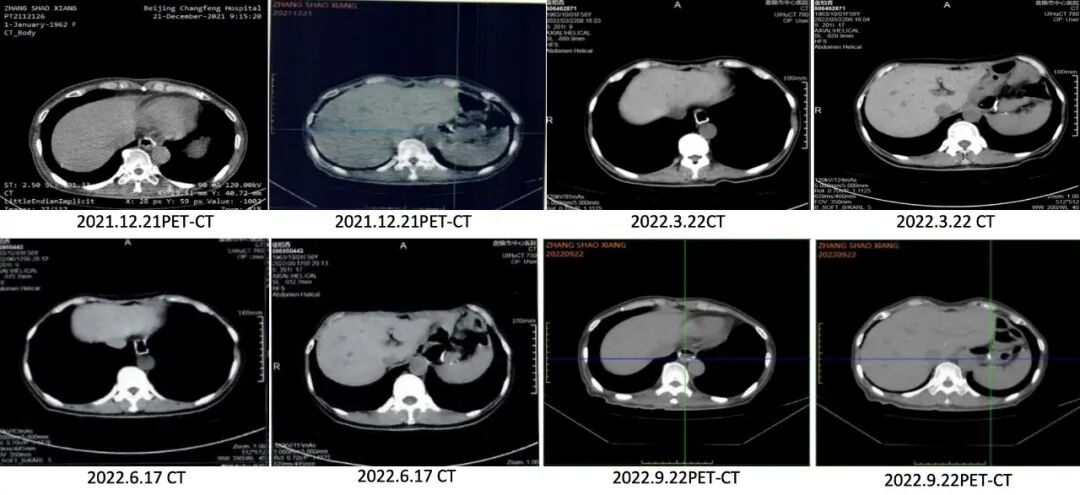
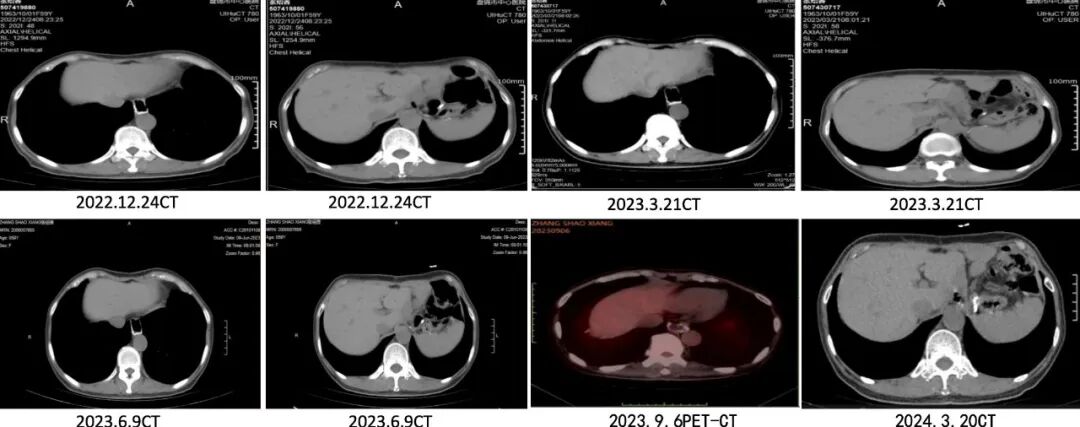
上腹部影像學顯示:2021.12示胃形態缺如,食管下段及上腹部腸管可見致密影,考慮術後改變,術區未見明顯復發徵象,2022.3至2024.3復查較前變化不明顯。
結論與點評
腫瘤治療是一場與時間賽跑的攻堅戰,需要在療效與安全性之間找到最佳平衡點。對於化療頻繁導致骨髓抑制的患者,vNKT細胞治療提供了一種全新的破局思路——既能精准清除腫瘤細胞,又能保護造血功能,為突破治療瓶頸開闢了一條希望之路。

參考文獻[1]趙中凱,王曄,劉鑫,等.內鏡黏膜下剝離與外科手術治療早期胃癌的療效與安全性分析[J].中國微創外科雜誌,2023,23(06):416-421.
升白指南:點擊閱讀《化療、放療後白細胞減少,如何升白?》,瞭解科學提升白細胞的方法,助您更好地應對治療挑戰。
抗癌支持:添加樂和小助手微信,獲取更多抗癌食譜,並加入患友群,與同路人分享經驗、互相鼓勵。
抗癌路上,您並不孤單。每一次治療選擇,都是向希望邁出的堅實一步。

掃描二維碼
與張明徽教授團隊溝通

樂和新醫創始人
清華大學醫學院免疫學博士,2002年發現vNKT細胞至今,張明徽教授帶領的研究團隊走過了20餘年的研究歷程,積累了700余例實體腫瘤的治療經驗,涉及幾乎所有常見實體腫瘤,研究結果充分證明vNKT在實體腫瘤治療中具有巨大價值。

適用於病理惡性程度較高或存在復發風險的術後患者;經化療、放療、靶向治療等常規治療腫瘤已基本控制但仍未達到治癒的患者;持續存在較高致癌因素的患者;放療、化療不耐受的患者。這些患者如果在傳統抗腫瘤治療後沒有進行有效的後續治療,復發、轉移或再發腫瘤將是大概率事件,在這種情況vNKT細胞治療是理想的後續治療手段,可顯著改善患者的預後。
點擊圖片查看往期精彩內容